2024年11月27日,国家药品监督管理局(NMPA)官网显示,已正式完全批准四川科伦博泰生物医药股份有限公司开发的注射用芦康沙妥珠单抗(SKB264/sac-TMT,商品名:佳泰莱®)用于既往至少接受过2种系统治疗(其中至少1种治疗针对晚期或转移性阶段)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者(CXSS2300093)。芦康沙妥珠单抗是一款靶向TROP2的抗体偶联药物(ADC),成为中国首个获批上市的国产创新TROP2 ADC。芦康沙妥珠单抗获批上市,将为我国晚期三阴性乳腺癌患者带来全新的治疗选择与希望!
在此重要时刻,特邀中山大学附属肿瘤医院王树森教授,寄语祝贺芦康沙妥珠获批晚期三阴性乳腺癌(TNBC)二线及以上适应证。 
OptiTROP-Breast01研究主要研究者王树森教授表示:热烈祝贺芦康沙妥珠单抗正式获得国家药品监督管理局批准上市用于晚期三阴性乳腺癌的治疗。芦康沙妥珠单抗是一种针对TROP2的抗体偶联药物,临床研究显示,与标准化疗相比,芦康沙妥珠单抗能显著提高晚期三阴性乳腺癌的生存率。因此,这一药物的获批为晚期三阴性乳腺癌的治疗提供了新的标准选择。
大家知道,因为缺乏相应的靶向治疗药物,晚期三阴性乳腺癌预后较差,现在随着芦康沙妥珠单抗的上市,对于晚期三阴性乳腺癌患者,我们有了更好的武器。特别期待芦康沙妥珠单抗能够在临床上有更多的使用经验和使用场景,也期待这一药物能在其他亚型的乳腺癌中,如激素受体阳性、HER2阴性的晚期乳腺癌,也能取得满意的效果。希望随着在临床上的广泛应用,芦康沙妥珠单抗能够造福广大的乳腺癌患者。
芦康沙妥珠单抗(SKB264/sac-TMT)
聚力创新,成就非凡
ADC由于能够对癌细胞进行精准打击,被称为“魔法子弹”,这种创新疗法的出现,为包括乳腺癌在内的许多癌症患者带来了新的治疗选择。芦康沙妥单抗正是一款TROP2 ADC明星产品,由科伦博泰自主研发。2022年5月,科伦博泰授予默沙东在大中华区以外的所有地区开发、制造及商业化芦康沙妥珠单抗(SKB264 /sac-TMT)的独家权利。
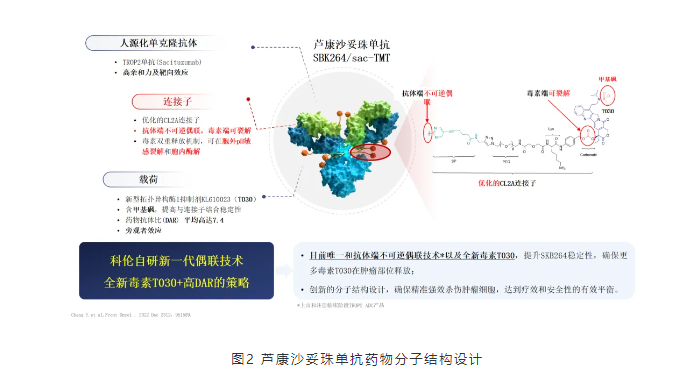
科伦博泰坚持从源头上创新,芦康沙妥珠单抗从设计之初就力求完美,采取当下最主流最成功的设计理念和策略,中等毒性的载药、高药物抗体比(DAR)、可裂解的连接子及可发挥旁观者效应。靶向TROP2的人源化单克隆抗体(Sacituzumab)通过创新的且经过优化的可裂解的连接子CL2A与自研的新型拓扑异构酶I抑制剂KL610023(T030)连接组成,药物抗体比平均高达7.4:1。该药的作用机理为,芦康沙妥珠单抗与肿瘤细胞表面的TROP2抗原特异性结合后被肿瘤细胞内吞,在溶酶体作用下释放T030,杀伤肿瘤细胞;T030穿透肿瘤细胞膜,发挥旁观者效应,进一步杀伤周围肿瘤细胞;在肿瘤高代谢所致的酸性环境中,芦康沙妥珠单抗连接子毒素端发生裂解,释放T030,杀伤肿瘤细胞。综上所述,芦康沙妥珠单抗通过三重机制精准强效的杀伤肿瘤细胞,兼顾疗效和安全性,达到全面平衡,实现“魔法子弹”的功效,药物分子结构和机制的优势最终转化成临床研究中更好的数据和患者生存获益。
OptiTROP-Breast01研究
卓尔不群,创造历史
芦康沙妥珠单抗本次获批是基于III期临床研究OptiTROP-Breast01的积极阳性结果。这是一项多中心、随机对照、开放标签的III期临床研究(NCT05347134),由中国医学科学院肿瘤医院徐兵河院士和江苏省人民医院殷咏梅教授共同牵头,立足于mTNBC治疗手段匮乏的临床难点,旨在评估芦康沙妥珠单抗相较于化疗(艾立布林、长春瑞滨、吉西他滨和卡培他滨),对于局部复发或转移性TNBC患者的有效性和安全性。

研究结果确证,芦康沙妥珠单抗疗效远优于现有标准药物,重塑晚期三阴性乳腺癌二线治疗新标准。与化疗相比,芦康沙妥珠单抗在无进展生存期(PFS)和总生存期(OS)上均显示出具有显著统计学意义和临床意义的改善。芦康沙妥珠单抗组的中位无进展生存期(mPFS)为6.7个月(HR:0.32;95% CI:0.22-0.44;p<0.00001),与化疗相比,疾病进展或死亡风险显著降低68%;中位总生存期(mOS)尚未达到,但已跨越疗效界值(0.0042),死亡风险显著降低47%(HR:0.53;95% CI: 0.36,-0.78;P = 0.0005);客观缓解率(ORR)为45.4%,mDOR为7.1月。整体安全性临床易于管控,最常见的是血液学不良反应,治疗相关不良反应(TRAE)导致的停药比例低(仅1.5%)。

芦康沙妥珠单抗研究展望
勇立潮头,全面奋进
对于HR+/HER2-转移性乳腺癌(mBC)芦康沙妥珠单抗同样表现抢眼,2023 年ESMO大会,公布了其用于经过多线治疗的HR+/HER2-mBC的初步结果(数据来自KL264-01篮子研究),疗效令人欣喜,ORR高达36.8%,mPFS长达11.1个月;同时,整体安全性可管可控,最常见的是血液学不良反应。不仅如此,2024年8月19日,芦康沙妥珠单抗用于治疗经EGFR-TKI和含铂化疗治疗失败的 EGFR突变局部晚期或转移性非小细胞肺癌(NSCLC)的新药申请(NDA)获NMPA药品审评中心(CDE)受理,并纳入优先审评。同年10月31日,芦康沙妥珠单抗用于治疗EGFR-TKI治疗进展的EGFR突变局部晚期或转移性NSCLC的新药申请获CDE受理并纳入优先审评。未来随着两项适应证的获批,芦康沙妥珠单抗有望改变EGFR-TKI耐药后晚期NSCLC患者的治疗格局。同时,芦康沙妥珠单抗在妇科肿瘤和消化道肿瘤也相继取得了出色的成果。芦康沙妥珠单抗展现出了同类最佳的潜质,立足于临床巨大的未被满足的治疗需求,科伦博泰携手默沙东已注册开展了17项III期临床试验(20241028 from ClinicalTrials.gov & Chinadrugtrials公开信息),探索芦康沙妥珠单抗在不同肿瘤、不同疾病阶段、不同治疗策略的疗效和安全性。随着临床试验项目不断地加码和加速,芦康沙妥珠单抗有望从「冲锋舟」化身「航空母舰」。 芦康沙妥珠单抗作为中国创新药出海的代表,成为现象级的产品也指日可待。

总而言之,芦康沙妥珠单抗的获批上市将改变晚期三阴性乳腺癌治疗格局,同时改善TROP2 ADC药物的临床可及性,为中国晚期TNBC患者带来更有效更安全的治疗选择。展望未来,芦康沙妥珠单抗有望惠及全球广大肿瘤患者,帮助患者延长生命和改善生活质量,奠定中国创新药在全球肿瘤研发和治疗领域的地位。