随着抗体偶联药物(ADC)在癌症治疗领域的不断突破,其已被认为是极具前景的创新疗法。近年来,靶向人类滋养层细胞表面抗原2(TROP2)的ADC药物在临床上展现出改善癌症患者预后的巨大潜能,且该疗法已在晚期三阴性乳腺癌(TNBC)的治疗中得到验证。作为中国首个原创的TROP2 ADC药物,芦康沙妥珠单抗已于11月28日获批上市用于局部晚期或转移性TNBC二线及以上治疗的适应症,为晚期TNBC患者提供全新的治疗选择。
更令人欣喜的是,TROP2 ADC芦康沙妥珠单抗在非小细胞肺癌(NSCLC)治疗领域的表现亦同样耀眼,其用于治疗经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)和含铂化疗治疗失败的局部晚期或转移性EGFR突变NSCLC的新药上市申请(NDA)已被国家药品监督管理局药品审评中心(CDE)纳入优先审评,另一项用于经EGFR-TKI治疗失败的局部晚期或转移性EGFR突变NSCLC的NDA也已被纳入优先审评,有望为此类患者提供新的治疗选择。此外,其联合免疫疗法亦在PD-L1阳性的局部晚期或转移性NSCLC一线治疗领域亦展现出治疗潜力。为此,【肿瘤资讯】特邀同济大学附属东方医院周彩存教授详细解读芦康沙妥珠单抗相关研究解读以及其在晚期肺癌患者中的治疗前景,以飨读者。

突破困境,TROP2 ADC芦康沙妥珠单抗助力EGFR-TKI耐药NSCLC人群获益
NSCLC患者EGFR-TKI耐药现状
在NSCLC靶向治疗领域,EGFR突变的识别标志着精准化治疗的重要进展。作为NSCLC靶向治疗的常见药物,EGFR-TKI的应用显著延长了EGFR突变阳性晚期NSCLC患者的无进展生存期(PFS)和总生存期(OS)。近年来EGFR-TKI不断更新迭代,三代TKI进一步提升了EGFR突变患者的一线治疗疗效,但获得性耐药的问题依然不可避免。EGFR-TKI的耐药机制复杂多样,主要包括EGFR依赖性耐药,如C797X突变、L718Q、EGFR扩增、G724S等,以及非EGFR依赖性耐药,如EGFR旁路信号激活、小细胞肺癌(SCLC)转化、PIK3CA突变或扩增等。这些耐药机制的复杂性要求临床上采取更为精细化的管理策略,也导致患者不得不找寻新的方法以求获得更多的生存空间。
此外,由于我国人口基数庞大,EGFR耐药问题则更为突出,患者耐药后的治疗需求尚不能完全满足。未来需要更加的深入研究以阐明耐药性机制,使耐药后的治疗模式更加精准,以为我国众多的EGFR耐药肺癌患者提供更多的治疗方案选择。
EGFR-TKI耐药后的探索
目前,针对EGFR-TKI耐药的研究主要集中在耐药后的靶向治疗、免疫治疗和ADC等方面。其中,ADC药物是目前的研究热点,随着TROP2成为肿瘤治疗的热门靶点之一,以芦康沙妥珠单抗为代表的TROP2 ADC药物逐渐在肿瘤领域显示出治疗优势。ADC药物通过特异性抗体与抗原的结合,实现了细胞毒药物在靶病灶部位的精准释放,这一机制不仅有效防治细胞毒药物在非靶部位脱落,从而避免对正常组织造成的毒性;而且还确保在靶病灶部位释放更高浓度的细胞毒药物,拓宽治疗窗从而发挥更强的抗肿瘤活性。
2024年美国癌症研究协会(AACR)年会上,芦康沙妥珠单抗用于经治晚期NSCLC患者的 II 期研究更新数据显示[1],中位随访时间达到17.2个月时,总人群的客观缓解率(ORR)达到43.6%,中位缓解持续时间(DoR)为9.3个月,中位PFS延长至7.2个月,中位OS为22.6个月。
值得一提的是,在EGFR-TKI治疗进展的EGFR突变患者队列中,芦康沙妥珠单抗单药的ORR高达60%,中位DoR为8.7个月,中位PFS长达11.5个月,中位OS为22.7个月[2]。这提示,芦康沙妥珠单抗单药治疗经治的EGFR突变患者获益更为显著。
以上卓越的II期研究数据仅为序幕,今年8月,芦康沙妥珠单抗治疗经治的EGFR突变NSCLC的OptiTROP-Lung03关键注册研究证实,芦康沙妥珠单抗在EGFR突变耐药人群中已经展现出显著的疗效,即与多西他赛相比,芦康沙妥珠单抗在ORR和PFS方面均显示出具有显著统计学意义和临床意义的显著获益。基于该项研究数据,目前其NDA已获正式受理。紧随其后,基于另一项OptiTROP-Lung04研究取得的积极结果,芦康沙妥珠单抗单药治疗经EGFR-TKI治疗后进展的局部晚期或转移性EGFR突变NSCLC的NDA也已获CDE正式受理并纳入优先审评。这两项NDA的优先审评意味着芦康沙妥珠单抗将在不久后将正式落地临床,并将成为我国首个获批用于治疗EGFR-TKI治疗失败NSCLC的TROP2 ADC,且有望优先成为EGFR靶向治疗失败后的后续治疗策略。
持续推进,TROP2 ADC为晚期NSCLC一线治疗带来新的机遇
芦康沙妥珠单抗联合免疫一线治疗NSCLC,患者生存获益显著
OptiTROP-Lung01研究旨在探索芦康沙妥珠单抗联合KL-A167(PD-L1抑制剂)一线治疗驱动基因阴性晚期NSCLC患者的疗效。研究共纳入了103例患者,分为两组,分别采用芦康沙妥珠单抗(5mg/kg Q3W)+KL-A167(1200mg Q3W)(队列1A)或芦康沙妥珠单抗(5mg/kg Q2W)+KL-A167(900mg Q2W)(队列1B)进行治疗。今年ASCO大会上公布的结果显示[3],队列1A和队列1B的中位随访时间分别为14.0个月和6.9个月。队列1A的ORR为48.6%,DCR为94.6%,中位PFS为15.4个月(95% CI:6.7,未达到),6个月PFS率为69.2%;队列1B的ORR为77.6%,疾病控制率(DCR)为100%,中位PFS未达到,6个月PFS率为84.6%。此外,亚组分析显示,队列1B中不同PD-L1表达水平、不同组织学类型(鳞癌/非鳞癌)患者均有一致的临床获益,且在PD-L1 TPS1%-49%和≥50%患者中,ORR更分别高达81.3%和87.0%。
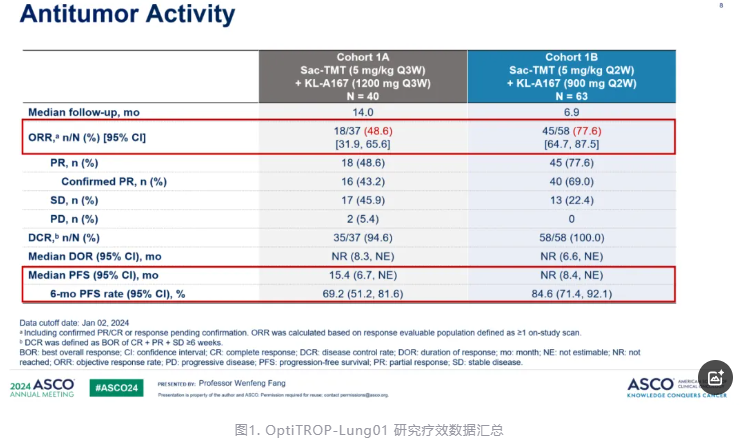
而在安全性方面,在1A/1B队列中,最常见的3级及以上治疗相关不良事件(TRAEs)主要以血液学不良事件为主,可控可管理。研究中未观察到治疗相关的停药或死亡。
本研究提示,芦康沙妥珠单抗联合KL-A167在初治晚期NSCLC中显示出有希望的疗效结果,安全性可控。
芦康沙妥珠单抗联合免疫治疗策略,前景广阔
在肺癌治疗领域,TROP2 ADC药物联合免疫治疗的探索已取得初步且令人鼓舞的成果。这种创新的联合治疗策略凭借其潜在的协同作用,已在多个探索性研究中得到了验证,预示着这将成为未来研究探索的重要方向。
目前在驱动基因阴性的早期和晚期NSCLC治疗领域,芦康沙妥珠单抗已有5项大型III期注册研究已经启动,未来期待研究结果能够为驱动基因阴性肺癌群体的多样化治疗提供循证医学证据。相信随着研究的不断推进,芦康沙妥珠单抗定能够在肺癌治疗中发挥更大的作用,为患者带来新的生机与希望。
令人振奋,芦康沙妥珠单抗将推动我国新药研发进展,为肿瘤治疗带来深远影响
目前,芦康沙妥珠单抗在局部晚期或转移性EGFR突变NSCLC的两项适应症已获CDE正式受理,并纳入优先审评。众所周知,NDA是药物获批上市前最重要的审批程序之一,NDA获正式受理,意味着芦康沙妥珠单抗将在不久后正式落地临床,有望为EGFR-TKI耐药的NSCLC患者提供更佳的治疗选择。
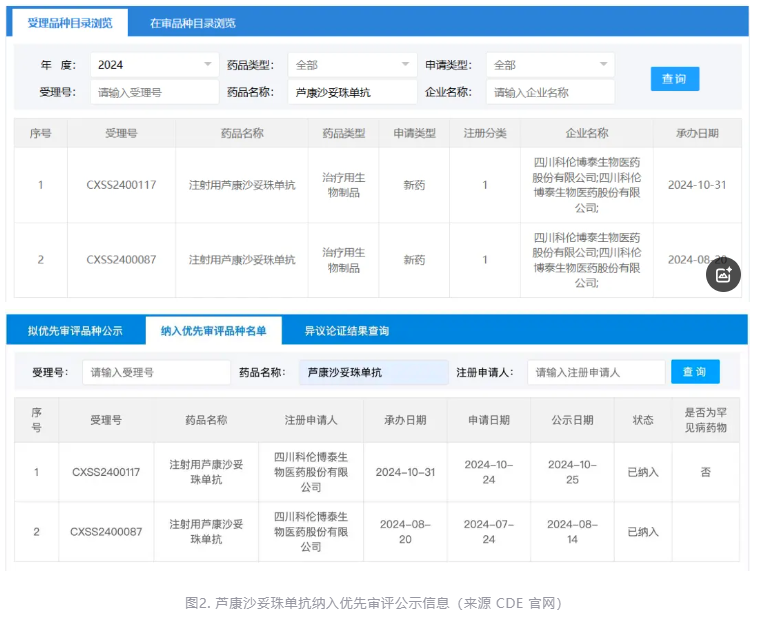
芦康沙妥珠单抗取得的成果,不仅彰显了我国在新药研发方面的创新实力和国际竞争力,还进一步肯定了我国科研人员的辛勤工作成果,也有力证明了我国新药研发的未来潜力。
更重要的是,越来越多创新药的快速审批和上市,将有助于提高我国更多肿瘤患者的生存获益,也是我国实现“健康中国2030”战略目标的重要组成部分。
综上,芦康沙妥珠单抗的成功不仅对肿瘤患者的个体化治疗有着直接的积极影响,也为中国的医药创新和国际化开辟了新的道路,同时对整个医药行业的发展和国家的公共卫生体系有着深远的意义。
参考文献
1. Liu Q, Yu S, Zhao W, et al. EGFR-TKI resistance via EGFR-independent signaling pathways[J]. Mol Cancer, 2018, 17(1): 53.
2. Fang WF, Cheng Y, Chen ZD,et al. Updated efficacy and safety of anti-TROP2 ADC SKB264 (MK-2870) for previously treated advanced NSCLC in Phase 2 study. 2024 AACR, Abstract CT247.
3. Fang WF, et al. Sacituzumab tirumotecan (SKB264/MK-2870) in combination with KL-A167 (anti-PD-L1) as first-line treatment for patients with advanced NSCLC from the phase II OptiTROP-Lung01 study. 2024 ASCO Oral Abstract Session LUNG CANCER—NON–SMALL CELL METASTATIC. Abstract 8502.